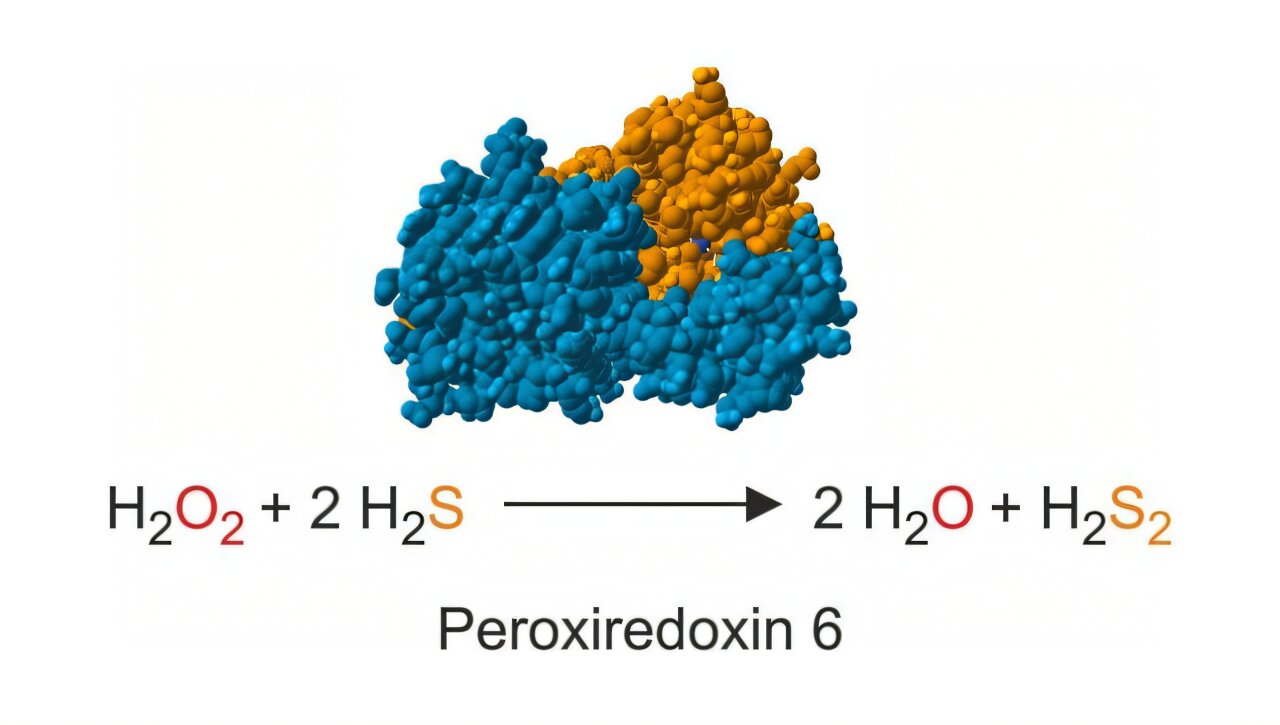
Peroksidazlar organizmalarda hidrojen peroksiti parçalayan enzimlerdir. 1998’deki keşiflerinden bu yana, bu reaksiyon için “peroksiredoksin 6 tipi” peroksidazların elektron kaynağı belirsizliğini korudu. RPTU’daki Profesör Marcel Deponte’nin araştırma grubu artık bu bilgi açığını kapattı. Araştırmacılar iki model organizmada (insanlar ve sıtma patojenleri) peroksiredoksin 6 tipi enzimlerin hidrojen sülfürün anyonu olan hidrosülfit ile hızla reaksiyona girdiğini gösterdi. Araştırma dergide yayımlandı İleri Bilim. Bulgular, peroksit ve sülfit metabolizması arasında önceden bilinmeyen bir bağlantıyı ortaya koyuyor.
Uzun yıllardır Deponte grubu, hidrojen peroksidi enzimatik olarak detoksifiye eden veya onu bir sinyal molekülüne dönüştüren peroksidazlar da dahil olmak üzere redoks enzimlerini karşılaştırmış ve karakterize etmiştir. Bu enzimler, indirgeyici bir maddeden hidrojen peroksite aktardıkları elektronlara ihtiyaç duyar. 1998’den beri bu alanda uzun süredir devam eden sorulardan biri, peroksiredoksin 6 tipi peroksidazların hangi indirgeyici ajanı kullandığıdır.
Doktora çalışması sırasında. Deponte laboratuvarındaki araştırmada Lukas Lang, peroksiredoksin 6 tipi enzimlerin, ilgili peroksidazlardan farklı olarak yaygın fizyolojik indirgeyici ajanlarla reaksiyona girmediğini gösterdi.
Kaiserslautern’den biyokimyacı şöyle açıklıyor: “Tüm canlı organizmalarda bulunan hidrojen sülfit veya sülfitleri indirgeyici ajanlar olarak test etme fikri, 2024 yılında diğer iki araştırma grubu bağımsız olarak peroksiredoksin 6 tipi peroksidazların hidrojen selenit ile reaksiyona girebileceğini keşfettiğinde hız kazandı.”
Peroksit metabolizması sülfit metabolizmasıyla buluşuyor
Hidrojen selenit ve hidrojen sülfür benzer kimyasal özelliklere sahiptir. Bununla birlikte, bu yaygın peroksidaz tipine sahip organizmaların tümü selenyum metabolizmasına sahip değildir; oysa tüm canlı organizmalar, sülfit metabolizmasına sahiptir. Hidrojen sülfür yalnızca kötü kokulu ve potansiyel olarak zehirli bir gaz değildir. Aynı zamanda bir sinyal molekülü olarak da görev yapar ve örneğin demir-kükürt enzim kümelerinde sülfit olarak protondan arındırılmış formda oluşur. Bu nedenle çalışmanın ilk yazarları Laura Leiskau ve Lukas Lang, başlangıçta sırf meraktan dolayı peroksiredoksin 6 tipi enzimlerin hidrojen sülfit ile reaksiyona girip girmediğini araştırdılar.

“Araştırmamız, insanlarda peroksiredoksin 6 tipi peroksidazların ve sıtma paraziti Plasmodium falciparum’un, hidrojen sülfürün anyonu olan hidrosülfit ile son derece hızlı reaksiyona girdiğini gösterdi. Bunun sonucunda hidrojen peroksit suya indirgenir ve potansiyel bir persülfit kaynağı olarak hidrojen disülfür oluşur. İkincisinin şu anda koruyucu bir işleve sahip olduğu düşünülüyor. Ayrıca, ilk olarak biz kazandık. Bu enzimlerin olağandışı katalitik döngüsünün ara maddelerine dair içgörüler” diye bitiriyor doktora öğrencisi Leiskau.
Kaiserslautern çalışma grubu böylece peroksit ve sülfit metabolizması arasında olası yeni bir enzimatik bağlantıyı göstermeyi başardı ve böylece persülfit biyokimyasının daha iyi anlaşılmasına katkıda bulundu.
İki model organizmadan elde edilen enzimler karşılaştırılabilir sonuçlar sağlar
Hızlı enzimatik reaksiyonları doğrudan ölçmek için Leiskau, araştırmasında durdurulan akış yöntemini kullandı. Bu yöntemde reaksiyon ortakları, yani enzim ve substratı bir spektrometre içerisinde çok hızlı bir şekilde karıştırılır. Araştırılan enzimin farklı durumları farklı floresans özelliklerine sahipse, kataliz sırasındaki olası değişiklikler bir floresans detektörü kullanılarak saniyenin binde biri aralığında takip edilebilir.
Ticari peroksit çözeltileri ve yüksek saflıkta karşılık gelen sülfit tuzları, hidrojen peroksit ve hidrosülfit kaynakları olarak görev yaptı. İnsandan ve sıtma parazitinden elde edilen gerekli miktardaki peroksiredoksin 6 tipi enzimler, Escherichia coli bakterisinin zararsız suşlarında rekombinant şekilde üretildi ve ardından saflaştırıldı.
Deponte, “İnsanlar ve sıtma parazitleri evrimsel olarak ilgisizdir ve tamamen farklı ökaryot gruplarına aittir. Sonuçlar oldukça karşılaştırılabilir olduğundan, hidrosülfürün diğer peroksiredoksin 6 tipi peroksidazlarla da çok hızlı reaksiyona girdiğini varsayıyoruz” diye açıklıyor Deponte.